

周菁
教授、系副主任
一、PI简介

周菁教授,北京大学基础医学院长聘教授
北京大学博雅特聘教授、学系副主任
血管稳态与重构全国重点实验室PI
国家自然科学基金杰出青年科学基金(青A)
优秀青年科学基金(青B)获得者
2006年在重庆大学生物工程学院获博士学位,随后在中国科学院上海生命科学研究院生物化学与细胞生物学研究所、台湾卫生研究院医学工程研究组、美国加州大学圣地牙哥分校医学与工程研究所接受博士后训练,自2011年在加州大学圣地牙哥分校医学与工程研究所任助理项目科学家,2014年以“北京大学百人计划”受聘于北京大学医学部。
二、研究方向与成果
周菁教授课题组主要从事力学生物学与血管疾病发病机制研究,围绕“机械力信号的感知与转导及其在血管重构中的作用”开展系统性工作。其研究方向及代表性成果如下:
一、机械力感知与相分离:揭示机械应力诱导蛋白质液-液相分离在血管重构中的作用。研究发现受体酪氨酸激酶DDR1、粘着斑蛋白Kindlin-2等力敏感分子在血流剪切力或基质刚度作用下发生相分离,通过调控力学信号转导通路影响血管稳态及动脉粥样硬化等血管疾病的发生与进展。
二、力学-表观遗传调控:提出并验证DNA甲基转移酶DNMT1在力学对细胞功能的表观遗传调控过程中的核心作用。证实基质刚度与血流扰动等机械力刺激通过DNA甲基化调控血管平滑肌细胞炎性反应、内皮间质转化及线粒体代谢,并发现线粒体DNA甲基化修饰影响细胞能量代谢与收缩功能。
三、细胞代谢重编程:明确力学信号对血管细胞代谢途径的影响及机制。研究显示几何约束通过线粒体DNA甲基化影响平滑肌能量代谢;MFN2通过调控PFK1稳定性抑制糖酵解过程,而cPLA2的力学激活可抑制脂肪酸氧化,这些机制在静脉移植物再狭窄等过程中具有功能意义。
此外,课题组关注新工具、新方法的开发与应用,如构建基于FRET的生物传感器用于活细胞中力学信号相关分子事件的动态监测,并探索利用力学响应性纳米递送系统对血流扰动相关病变区域进行靶向干预。
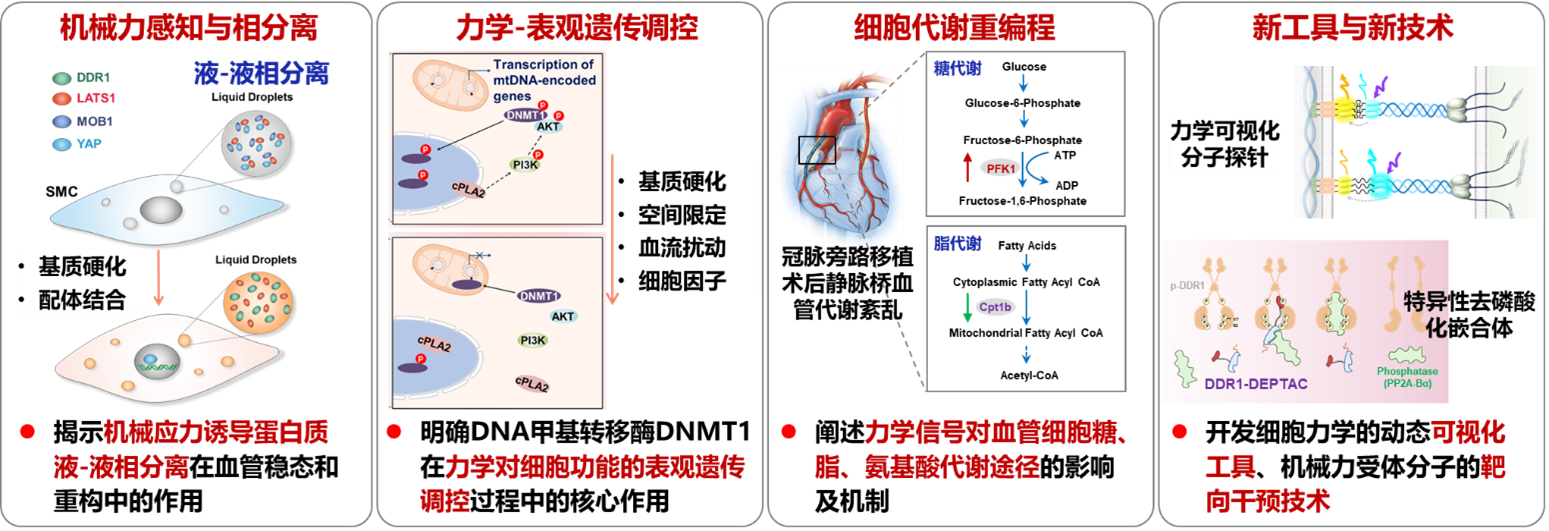
主要研究方向与成果
三、学术兼职
中国解剖学会血管分会副主任委员、中国生理学会基质生物学专业委员会委员、中国生物医学工程学会生物力学专业委员会
委员、中国生物物理学会力生物学分会/单分子生物学分会委员等。
四、主持基金项目
主持国家自然科学基金杰出青年科学基金、优秀青年科学基金、青年科学基金项目、重大研究计划项目(2项)、面上项目(3项),北京市自然科学基金非共识创新项目、面上项目等。
五、主要论文(全部Peer-review论文见ORCID 0000-0002-2211-4901)
Liu JY#*, Chen J#, Chen QY, Li HB, Gui LX, Zhou J*, Lin MJ*. Liquid-liquid phase separation of EphB4 drives pulmonary hypertension via YAP activation. Cell Rep. 45(2):116992. 2026.
Liu Y, Zhao C, Liang Z, Xu Y, Liu J, Yao W*, Zhou J*. APEX1-STAT3 signaling mediates the force-coordinated endothelial regeneration. Cell Mol Life Sci. 82(1):321. 2025.
Fan L, Tang Y, Liu J, Liu Y, Xu Y, Liu J, Liu H, Pang W, Guo Y, Yao W, Zhang T*, Peng Q*, Zhou J*. Mechanical Activation of cPLA2 Impedes Fatty Acid β-Oxidation in Vein Grafts. Adv Sci (Weinh). e2411559. 2025.
Ma N, Wu F, Liu J, Wu Z, Wang L, Li B, Liu Y, Dong X, Hu J, Fang X, Zhang H, Ai D, Zhou J*, Wang X*. Kindlin-2 Phase Separation in Response to Flow Controls Vascular Stability. Circ Res. 135(12):1141-1160. 2024.
Liu J#, Li Q#, Wang J#, Qiu J*, Zhou J*, Peng Q*. Genetically Encoded Fluorescence Resonance Energy Transfer Biosensor for Live-Cell Visualization of Lamin A Phosphorylation at Serine 22. Biomater Res. 28:0091. 2024.
Liu J#, Zhao C#, Xiao X, Li A, Liu Y, Zhao J, Fan L, Liang Z, Pang W, Yao W, Li W*, Zhou J*. Endothelial discoidin domain receptor 1 senses flow to modulate YAP activation. Nat Commun. 14(1):6457. 2023.
Liu J#, Wang J#, Liu Y, Xie S, Zhang J, Zhao C, Zhou Y, Pang W, Yao W, Peng Q, Wang X*, Zhou J*. Liquid-liquid phase separation of DDR1 counteracts the Hippo pathway to orchestrate arterial stiffening. Circ Res. 132(1):87-105. 2023.
Zhao J, Zhao C, Yang F, Jiang Z, Zhu J, Yao W, Pang W, Zhou J*. DNMT1 mediates the disturbed flow-induced endothelial to mesenchymal transition through disrupting b-alanine and carnosine homeostasis. Theranostics. 13(13):4392-4411. 2023.
Zhang J, Xie S, Wang J, Liu J, Liu Y, Zhou S, Li X, Han L, Pang W, Yao W, Fu Y, Kong W, Ye M*, Zhou J*. Echinatin maintains glutathione homeostasis in vascular smooth muscle cells to protect against matrix remodeling and arterial stiffening. Matrix Biol. 119:1-18. 2023.
Zhao C#, Yang Q#, Tang R#, Li W, Wang J, Yang F, Zhao J, Zhu J, Pang W, Li N, Zhang X, Tian XY, Yao W*, Zhou J*. DNA methyltransferase 1 deficiency improves macrophage motility and wound healing by ameliorating cholesterol accumulation. NPJ Regen Med. 8(1):29. 2023.
Zhao CR#, Li J#, Jiang ZT#, Zhu JJ, Zhao JN, Yang QR, Yao WJ, Pang W, Li N, Yu M*, Gan Y*, Zhou J*. Disturbed flow-facilitated margination and targeting of nanodisks protect against atherosclerosis. Small. e2204694. 2022.
Liu H#, Liu Y#, Wang H, Zhao Q, Zhang T, Xie SA, Liu Y, Tang Y, Peng Q, Pang W, Yao W, Zhou J*. Geometric Constraints Regulate Energy Metabolism and Cellular Contractility in Vascular Smooth Muscle Cells by Coordinating Mitochondrial DNA Methylation. Adv Sci (Weinh). e2203995. 2022.
Tang Y, Jia Y, Fan L, Liu H, Zhou Y, Wang M, Liu Y, Zhu J, Pang W*, Zhou J*. MFN2 Prevents Neointimal Hyperplasia in Vein Grafts via Destabilizing PFK1. Circ Res. 130(11):e26-e43.2022.
Wang J#, Xie S#, Li N, Zhang T, Yao W, Zhao H, Pang W, Han L, Liu J, Zhou J*. Matrix stiffness exacerbates the proinflammatory responses of vascular smooth muscle cell through the DDR1-DNMT1 mechanotransduction axis. Bioact Mater. 17:406-424. 2022.
Zhao CR, Yang FF, Cui QH, Wang D, Zhou YR, Li YS, Zhang YP, Tang RZ, Yao WJ, Wang X, Pang W, Zhao JN, Jiang ZT, Zhu JJ, Chien S*, Zhou J*. Vitexin Inhibits APEX1 to Counteract the Flow-Induced Endothelial Inflammation. Proc Natl Acad Sci U S A. 118(48): e2115158118, 2021.
Liu YF#, Zhu JJ#, Tian XY, Liu H, Zhang T, Zhang YP, Xie SA, Zheng M, Kong W, Yao WJ, Pang W, Zhao CR, Tang YJ, Zhou J*. Hypermethylation of Mitochondrial DNA in Vascular Smooth Muscle Cells Impairs Cell Contractility. Cell Death Dis. 11 (1), 35, 2020.
Xie SA, Zhang T, Wang J, Zhao F, Zhang YP, Yao WJ, Hur SS, Yeh YT, Pang W, Zheng LS, Fan YB, Kong W, Wang X, Chiu JJ, Zhou J*. Matrix stiffness determines the phenotype of vascular smooth muscle cell in vitro and in vivo: Role of DNA methyltransferase 1. Biomaterials. 155:203-216. 2018
Zhu JJ#, Liu YF#, Zhang YP, Zhao CR, Yao WJ, Li YS, Wang KC, Huang TS, Pang W, Wang XF, Wang X, Chien S*, Zhou J*. VAMP3 and SNAP23 mediate the disturbed flow-induced endothelial microRNA secretion and smooth muscle hyperplasia. Proc Natl Acad Sci U S A. 114(31):8271-8276, 2017.
六、课题组成员
周菁 教授
姚伟娟 副教授
韩丽丽 主管技师
研究生:周爽、耿学妤、徐艺玮、桂克、梁振辉、沈宇航、赵頔、冯宇婧、文佳怡、吴梓纯、胡皖豫、岳泽君、韩啸、于开元等

课题组成立十周年合影留念
七、联系方式
周菁
Office: 生理楼,306室
Email: jzhou@bjmu.edu.cn
Phone: 010-82801447
姚伟娟
Office: 生理楼,312室
Email: weijuanyao@bjmu.edu.cn
Phone: 010-82802419
韩丽丽
Office: 生理楼,303室
研究生
Office: 生理楼,308、309室

